 (资料图片仅供参考)
(资料图片仅供参考)
1、试题答案:(1)由于锌比铜活泼,所以锌作负极,所以消耗的金属为锌.锌失电子生成锌离子进入溶液。
2、电极反应式为锌片:Zn-2e-=Zn 2+,铜片上氢离子得电子生成氢气,所以电极反应式为:铜片:2H++2e-=H2↑.总反应:Zn+2H+=H2↑+Zn 2+ 65g 22.4L 9.75g 3.36L所以消耗金属的质量为9.75g.故答案为9.75g.(2)Zn+2H+=H2↑+Zn2+转移电子 22.4L 2mol 3.36L 0.3mol所以转移电子的物质的量为0.3mol。
3、即1.806×1023个.故答案为1.806×1023个.(3)根据氢原子守恒,H+全部由H2SO4提供,所以n(H2)=n(H2SO4)=0.15molc(H2SO4)=0.15mol0.2L=0.75mol/L故答案为0.75mol/L.。
本文到此分享完毕,希望对大家有所帮助。




 中国无人驾驶技术初创公司文远知行考虑IPO 最早于今年上市
中国无人驾驶技术初创公司文远知行考虑IPO 最早于今年上市
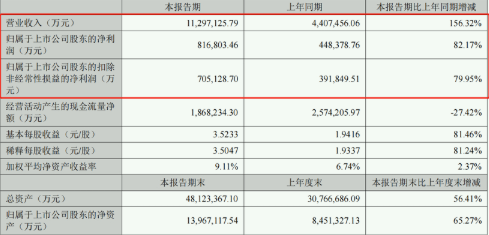 宁德时代上半年营业收入同比增156.32% 研发投入逼近同期净利
宁德时代上半年营业收入同比增156.32% 研发投入逼近同期净利
 兰博基尼上半年业绩创纪录 上半年生产5090辆汽车
兰博基尼上半年业绩创纪录 上半年生产5090辆汽车
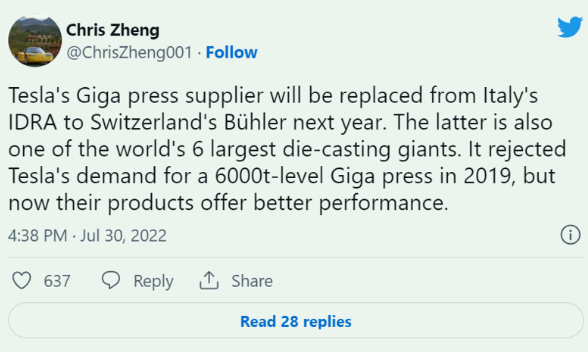 传特斯拉或引入另一家压铸机供应商 不会取消与IDRA合作
传特斯拉或引入另一家压铸机供应商 不会取消与IDRA合作
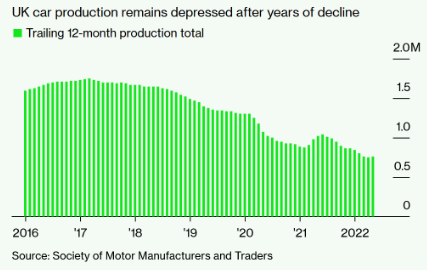 高油价有助于加速向电动汽车转型 英国5月汽车产量同比增13%
高油价有助于加速向电动汽车转型 英国5月汽车产量同比增13%